Resumen:
La respuesta inmunitaria innata desempeña un papel crucial en la detección y neutralización de agentes patógenos, así como en la reparación de tejidos dañados. Esta revisión explora los mecanismos mediante los cuales los patrones moleculares asociados a patógenos (PAMP), los patrones moleculares asociados a daño (DAMP), los receptores de reconocimiento de patrones (PRR) y los inflamasomas orquestan una respuesta inmunitaria coordinada frente a la invasión microbiana y al daño tisular.
Introducción:
El sistema inmunitario innato constituye la primera línea de defensa del organismo contra las infecciones y el daño tisular. El reconocimiento rápido y eficaz de las señales de peligro, ya provengan de patógenos o de células huésped dañadas, es esencial para activar las respuestas inmunitarias apropiadas. Este reconocimiento está mediado por un conjunto complejo de receptores y vías de señalización que implican los PAMP, los DAMP, los PRR y los inflamasomas:
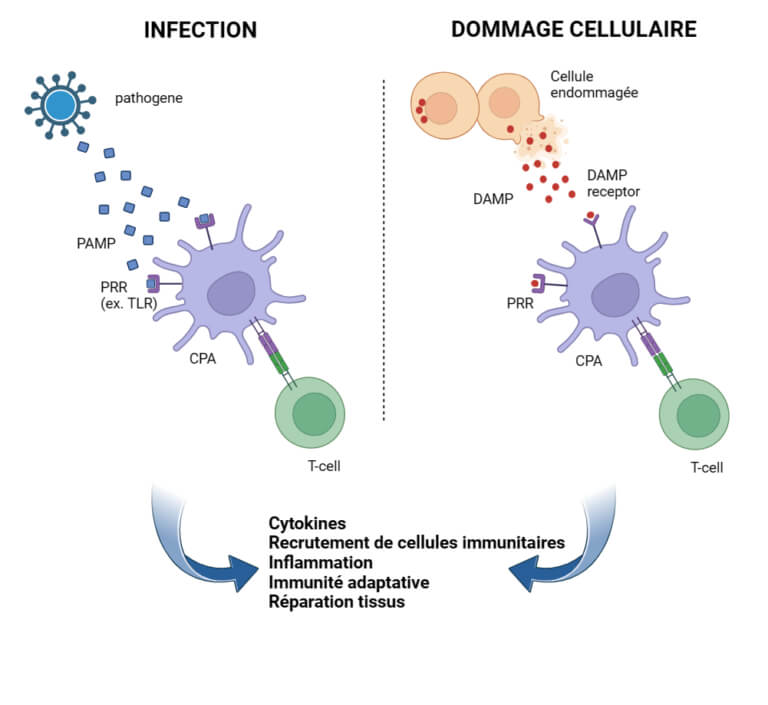
- PAMP y DAMP: desencadenantes de la respuesta inmunitaria
Los PAMP son motivos moleculares conservados presentes en los agentes patógenos, mientras que los DAMP son moléculas liberadas por las células huésped en respuesta a un daño. Ambos sirven como señales de alerta que activan el sistema inmunitario innato. - PRR: los sensores de peligro
Los PRR son una clase diversificada de receptores que detectan los PAMP y los DAMP. Entre los PRR, los receptores tipo Toll (TLR) y los receptores tipo NOD (NLR) son particularmente importantes por su capacidad para iniciar respuestas inflamatorias y antivirales.
- El inflamasoma: un complejo proteico clave en la respuesta inflamatoria
Los inflamasomas son complejos proteicos citosólicos que desempeñan un papel central en la regulación de la inflamación. Su activación por PAMP, DAMP u otras señales de estrés conduce a la maduración y secreción de citocinas proinflamatorias, especialmente IL-1β e IL-18.
Mecanismos de interacción y vías de señalización
La comprensión de los mecanismos de interacción entre los PAMP, DAMP, PRR e inflamasomas, así como de las vías de señalización implicadas, es crucial para dilucidar la complejidad de la respuesta inmunitaria innata. Estas interacciones orquestadas desencadenan una serie de eventos celulares que conducen a la activación de respuestas inmunitarias específicas y adaptativas.
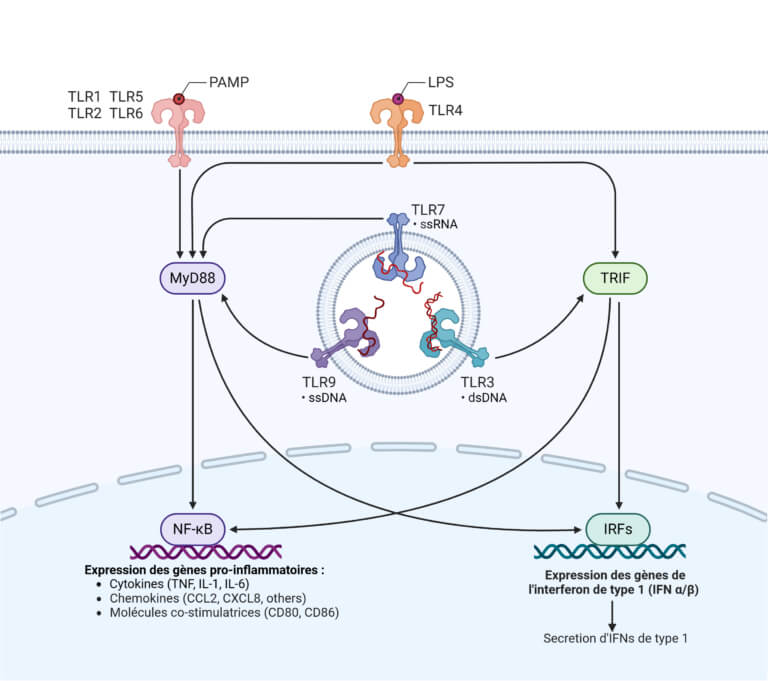
Activación de los PRR por los PAMP y DAMP
Los PRR, como los TLR y NLR, reconocen específicamente los PAMP y DAMP, lo que desencadena una cascada de señalización intracelular. Los TLR, por ejemplo, están situados en la superficie celular o en los endosomas y reconocen motivos específicos de PAMP y DAMP. La unión de un TLR a su ligando conduce a la activación de la vía dependiente de MyD88 o dependiente de TRIF, resultando en la translocación del factor de transcripción NF-κB al núcleo y en la expresión de genes proinflamatorios.
Papel de los NLR y activación del inflamasoma
Los NLR desempeñan un papel central en la formación del inflamasoma. La activación de NLRP3, un miembro de la familia de los NLR, por PAMP, DAMP o señales de estrés celular, conduce al ensamblaje del inflamasoma NLRP3. Este complejo recluta el adaptador ASC y la pro-caspasa-1, facilitando la conversión de la pro-caspasa-1 en caspasa-1 activa. La caspasa-1 cataliza entonces la maduración de IL-1β e IL-18, citocinas clave en la mediación de la respuesta inflamatoria.
Señalización posterior y respuestas inmunitarias
La señalización posterior a la activación de los PRR y del inflamasoma implica varias vías, incluida la vía JAK-STAT, que es esencial para la producción de interferones (IFN) de tipo I y tipo II en respuesta a las infecciones virales. Estas vías contribuyen a un estado antiviral, estimulan la presentación del antígeno y facilitan la comunicación entre la inmunidad innata y adaptativa.
Regulación de las respuestas inmunitarias
La regulación de estas respuestas está asegurada por mecanismos de retroalimentación negativa y moduladores postraduccionales, que garantizan que la respuesta inmunitaria sea proporcional a la amenaza y evitan daños excesivos a los tejidos huésped. Las proteínas de la familia SOCS, por ejemplo, son inducidas por citocinas e inhiben la señalización JAK-STAT para limitar las respuestas inflamatorias.
Implicaciones clínicas y perspectivas:
La comprensión profunda de la interacción entre los PAMP, DAMP, PRR e inflamasomas abre vías prometedoras para el desarrollo de nuevas estrategias terapéuticas. El enfoque BI(G)MED dirigido a modular estas interacciones mejora las respuestas inmunitarias contra las infecciones, reduce las respuestas inflamatorias patológicas y favorece la reparación tisular.
Para profundizar, aquí se presentan algunas publicaciones importantes en el campo:
- Janeway CA Jr, Medzhitov R. “Innate Immune Recognition.” Annual Review of Immunology. 2002;20:197-216.
Un artículo fundacional que describe cómo el sistema inmunitario reconoce los agentes patógenos a través de los PRR. - Kumar H, Kawai T, Akira S. “Pathogen Recognition by the Innate Immune System.” International Reviews of Immunology. 2011;30(1):16-34.
Este artículo proporciona una visión general completa sobre el reconocimiento de patógenos por el sistema inmunitario innato, haciendo hincapié en los PRR. - Takeuchi O, Akira S. “Pattern Recognition Receptors and Inflammation.” Cell. 2010;140(6):805-820.
Un artículo clave sobre el papel de los receptores de reconocimiento de patrones en el inicio de las respuestas inflamatorias. - Medzhitov R. “Origin and Physiological Roles of Inflammation.” Nature. 2008;454:428-435 .
Explora los orígenes y los papeles fisiológicos de la inflamación, ofreciendo un contexto importante para comprender la activación de los inflamasomas. - Schroder K, Tschopp J. “The Inflammasomes.” Cell. 2010;140(6):821-832.
Una revisión fundamental sobre los inflamasomas, su mecanismo de acción y su importancia en las enfermedades humanas. - Latz E, Xiao TS, Stutz A. “Activation and Regulation of the Inflammasomes.” Nature Reviews Immunology. 2013;13(6):397-411.
Describe en detalle la activación y regulación de los inflamasomas, subrayando su papel central en la inmunidad innata. - Rock KL, Latz E, Ontiveros F, Kono H. “The Sterile Inflammatory Response.” Annual Review of Immunology. 2010;28:321-342.
Este artículo explora la respuesta inflamatoria estéril, incluido el papel de los DAMP en el inicio de la inflamación sin la presencia de patógenos. - Bianchi ME. “DAMPs, PAMPs and Alarmins: All We Need to Know About Danger.” Journal of Leukocyte Biology. 2007;81(1):1-5.
Una visión esclarecedora sobre las moléculas de peligro, incluidos los DAMP y PAMP, y su importancia en la respuesta inmunitaria.