Zusammenfassung:
Der Einzelnukleotid-Polymorphismus (SNP) ist eine genetische Variation, die ein einzelnes Nukleotid betrifft. Manchmal ist er stumm, kann aber auch eine Veränderung des vom betroffenen Gen kodierten Proteins bewirken. SNPs sind im Genom sehr häufig und es wurde gezeigt, dass sie an einer Vielzahl von Erkrankungen beteiligt sind. Wir geben hier eine nicht erschöpfende Übersicht über ihre Rolle bei stressbedingten Angststörungen.
Was ist ein Einzelnukleotid-Polymorphismus?
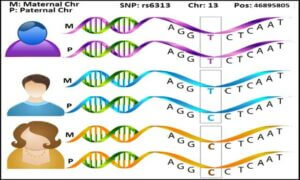
Ein Einzelnukleotid-Polymorphismus oder Single Nucleotide Polymorphism (SNP) ist eine genetische Variation, die auftritt, wenn sich ein einzelnes Nukleotid (A, T, C oder G) im Genom zwischen Mitgliedern einer Spezies oder zwischen gepaarten Chromosomen bei einem Individuum unterscheidet. SNPs sind die häufigsten Arten genetischer Variationen beim Menschen und können etwa alle 300 bis 1.000 Basen entlang des menschlichen Genoms gefunden werden.
SNPs spielen eine entscheidende Rolle in der Genetik, da sie beeinflussen können, wie eine Person auf Krankheiten, Medikamente, Umweltgifte und sogar Nährstoffe reagiert. Einige SNPs verursachen keine beobachtbare Veränderung in der Funktion eines Gens, während andere einen erheblichen Einfluss auf die Gesundheit oder Entwicklung einer Person haben können. Sie werden in der Forschung verwendet, um Gene zu identifizieren, die mit bestimmten Krankheiten assoziiert sind, und können als biologische Marker dienen, um die genetische Anfälligkeit für bestimmte Erkrankungen vorherzusagen. SNPs können auch in der personalisierten Medizin von Bedeutung sein, da die Kenntnis der spezifischen Variationen eines Patienten dazu beitragen kann, seine Behandlung zu individualisieren.
Nachweistechniken
Mehrere Techniken werden zum Nachweis von SNPs verwendet, jede mit ihren eigenen Vorteilen und Einschränkungen. Hier sind einige der gängigsten Methoden:
- DNA-Sequenzierung: Dies ist die präziseste Methode zur Identifizierung von SNPs. Die Sequenzierung der nächsten Generation (NGS) ermöglicht es, große Regionen des Genoms schnell und zu relativ geringen Kosten zu sequenzieren, wodurch der Nachweis von Millionen von SNPs in einer einzigen Probe möglich wird.
- Echtzeit-PCR (qPCR): Diese Technik amplifiziert die Ziel-DNA und verwendet sequenzspezifische fluoreszierende Sonden, um das Vorhandensein oder Fehlen von SNPs nachzuweisen. Sie wird häufig für die Analyse spezifischer SNPs verwendet und nicht für großflächiges Screening.
- Hybridisierung auf DNA-Chip: DNA-Chips oder Microarrays ermöglichen die gleichzeitige Analyse von Tausenden bis Millionen von SNPs. Die DNA des Probanden wird auf einem Chip hybridisiert, der Sonden enthält, die spezifisch für verschiedene SNP-Variationen sind. Die Regionen, in denen die DNA mit dem Chip hybridisiert, zeigen an, welche SNPs vorhanden sind.
- Primer-Extensionsanalyse: Diese Methode verwendet einen sequenzspezifischen Primer, der sich unmittelbar vor dem SNP anlagert. Die Extension des Primers durch eine DNA-Polymerase in Gegenwart markierter Nukleotide ermöglicht den Nachweis des Nukleotids an der Position des SNP.
- Polyacrylamid-Gelelektrophorese: Für bestimmte Arten von SNPs kann die Elektrophorese Variationen in Größe oder elektrischer Ladung unterscheiden, die aus dem Vorhandensein des SNP resultieren. Dies ist eine ältere Technik, die derzeit aufgrund ihrer geringen Durchsatzkapazität und geringeren Sensitivität im Vergleich zu modernen Methoden weniger für den Nachweis von SNPs verwendet wird.
Jede Methode hat ihre spezifischen Anwendungen, abhängig von den Anforderungen der Studie, der Anzahl der zu analysierenden SNPs, der erforderlichen Präzision und dem verfügbaren Budget.
SNP und stressbedingte Angststörungen
SNPs wurden umfassend untersucht, um ihre Rolle bei der Anfälligkeit für psychische Störungen wie Stress und Depression zu verstehen. Die Beziehung zwischen SNPs und diesen Störungen ist komplex und beinhaltet Wechselwirkungen zwischen mehreren Genen und der Umwelt. Hier ist eine Zusammenfassung der aktuellen Erkenntnisse über die wichtigsten SNPs, die mit Stress und Depression assoziiert sind:
- Gen SERT (SLC6A4)
Das Gen SERT, auch bekannt als SLC6A4, kodiert für den Serotonintransporter, der für die Regulation der Stimmung entscheidend ist. Ein gut untersuchter SNP in der Promotorregion dieses Gens ist der 5-HTTLPR. Er existiert in zwei Hauptallelen: dem langen Allel (L) und dem kurzen Allel (S). Das S-Allel ist mit einer geringeren Transkriptionsaktivität des SERT-Gens verbunden, was zu einer Verringerung der Serotoninwiederaufnahme führt und mit einer erhöhten Anfälligkeit für Stress und Depression in Verbindung gebracht wurde, insbesondere in Gegenwart von Umweltstressfaktoren. - Gen BDNF (Brain-Derived Neurotrophic Factor)
BDNF spielt eine Schlüsselrolle beim Überleben von Neuronen, bei Wachstum und Differenzierung sowie bei der synaptischen Plastizität. Der SNP Val66Met (rs6265) im BDNF-Gen, bei dem eine Aminosäure Valin (Val) durch Methionin (Met) ersetzt wird, wurde mit einer veränderten Gehirnfunktion und einem erhöhten Risiko für psychiatrische Störungen, einschließlich Stress und Depression, in Verbindung gebracht. Personen, die das Met-Allel tragen, können eine Verringerung der BDNF-Aktivität aufweisen, was die Stressresilienz negativ beeinflussen und die Anfälligkeit für Depressionen erhöhen könnte. - Gen FKBP5
FKBP5 reguliert die Empfindlichkeit der Glukokortikoidrezeptoren, die eine zentrale Rolle bei der Stressreaktion spielen. Varianten im FKBP5-Gen wurden mit einer verstärkten Stressreaktion und einem erhöhten Risiko für die Entwicklung stressbedingter Störungen wie der posttraumatischen Belastungsstörung (PTBS) und Depression in Verbindung gebracht. Diese Varianten können beeinflussen, wie das Individuum auf Stress reagiert und seine Emotionen reguliert. - Gen CRHR1
Das Gen CRHR1 kodiert für den Corticotropin-Releasing-Hormon-Rezeptor, der eine Rolle bei der Stressreaktion des Organismus spielt. SNPs in diesem Gen wurden mit einer erhöhten Anfälligkeit für Stress und Depression in Verbindung gebracht. Variationen in CRHR1 können die Stressreaktion beeinflussen, indem sie die Aktivierung der Hypothalamus-Hypophysen-Nebennierenrinden-Achse (HPA) verändern, was sich auf die Cortisolspiegel und folglich auf die Stressreaktion auswirkt. - Gen ADORA2A
Das Gen ADORA2A kodiert für den Adenosin-A2A-Rezeptor, ein Protein, das an verschiedenen physiologischen Prozessen beteiligt ist, einschließlich der Modulation der Neurotransmission, Entzündung und Stressreaktion. Einzelnukleotid-Polymorphismen (SNPs) im Gen ADORA2A wurden auf ihre potenzielle Assoziation mit verschiedenen psychiatrischen Erkrankungen, einschließlich Stress und Depression, untersucht.
Der SNP rs5751876 ist einer der am meisten untersuchten im Gen ADORA2A. Die T-Variante wurde bei bestimmten Personen mit erhöhter Angst und einer verstärkten Stressreaktion in Verbindung gebracht. Diese Variation könnte die Wirkung von Adenosin auf die A2A-Rezeptoren modulieren und dadurch die dopaminerge Neurotransmission und die Stressreaktion beeinflussen.
Der Nachweis der Rolle dieser SNPs bei stressbedingten Erkrankungen ist eine mühsame Arbeit. Die Forschung hat noch nicht alle identifiziert. Man muss sich auch der Bedeutung von Umweltfaktoren für die pathologische Expression dieser SNPs bewusst sein. Tatsächlich sind SNPs als Anfälligkeitsfaktoren für eine bestimmte Erkrankung zu verstehen. Umweltfaktoren wirken dann als Auslöser oder Verstärker dieser genetischen Anfälligkeit. Personen, die SNPs tragen, die ihre Anfälligkeit für Angst oder Depression erhöhen, könnten nur in Gegenwart spezifischer Stressfaktoren Symptome zeigen, wie traumatische Lebensereignisse oder chronische Stressbelastung.
Für weiterführende Informationen einige interessante Referenzen:
- Caspi, A., et al. (2003). Influence of Life Stress on Depression: Moderation by a Polymorphism in the 5-HTT Gene. Science, 301(5631), 386-389.
Diese klassische Studie untersucht, wie der Polymorphismus 5-HTTLPR im Gen SLC6A4 die Wirkung von erlebtem Stress auf das Depressionsrisiko moderiert. - Berton, O., & Nestler, E.J. (2006). New approaches to antidepressant drug discovery: beyond monoamines. Nature Reviews Neuroscience, 7(2), 137-151.
Diese Übersichtsarbeit untersucht Mechanismen jenseits der monoaminergen Theorie der Depression, einschließlich der Rolle von BDNF und anderen neurotrophen Faktoren. - Binder, E.B., et al. (2008). Association of FKBP5 Polymorphisms and Childhood Abuse With Risk of Posttraumatic Stress Disorder Symptoms in Adults. JAMA, 299(11), 1291-1305 .
Diese Forschung stellt einen Zusammenhang zwischen Varianten des FKBP5-Gens, Stressexposition in der Kindheit und dem späteren Risiko für die Entwicklung einer PTBS her.