Zusammenfassung:
Die angeborene Immunantwort spielt eine entscheidende Rolle bei der Erkennung und Neutralisierung von Krankheitserregern sowie bei der Reparatur von geschädigtem Gewebe. Diese Übersicht untersucht die Mechanismen, durch die Pathogen-Associated Molecular Patterns (PAMP), Damage-Associated Molecular Patterns (DAMP), Pattern Recognition Receptors (PRR) und Inflammasome eine koordinierte Immunantwort auf mikrobielle Invasion und Gewebeschäden orchestrieren.
Einleitung:
Das angeborene Immunsystem stellt die erste Verteidigungslinie des Organismus gegen Infektionen und Gewebeschäden dar. Die schnelle und effiziente Erkennung von Gefahrensignalen, ob sie nun von Krankheitserregern oder geschädigten Wirtszellen stammen, ist essenziell für die Aktivierung angemessener Immunantworten. Diese Erkennung wird durch ein komplexes Ensemble von Rezeptoren und Signalwegen vermittelt, an denen PAMP, DAMP, PRR und Inflammasome beteiligt sind:
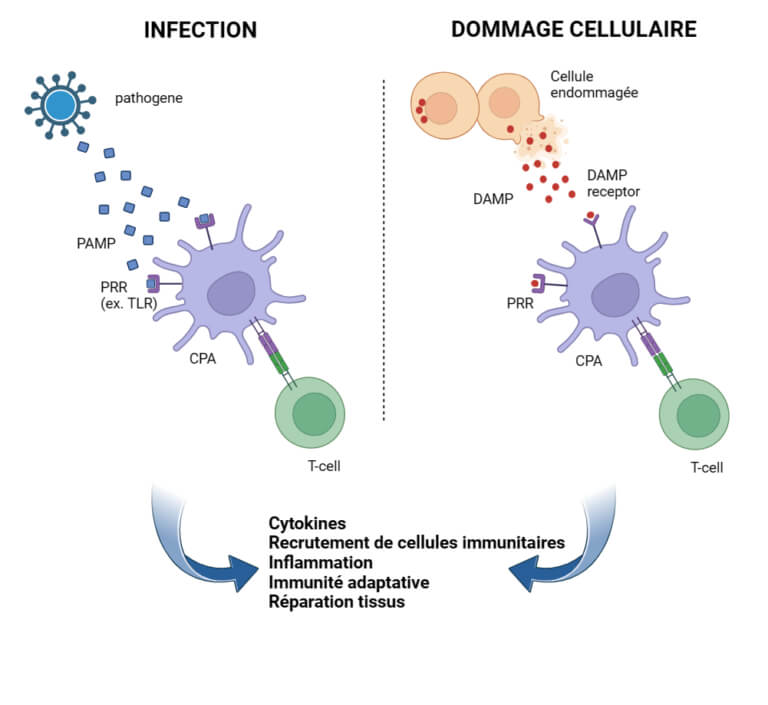
- PAMP und DAMP: Auslöser der Immunantwort
PAMP sind konservierte molekulare Muster, die auf Krankheitserregern vorhanden sind, während DAMP Moleküle sind, die von Wirtszellen als Reaktion auf eine Schädigung freigesetzt werden. Beide dienen als Warnsignale, die das angeborene Immunsystem aktivieren. - PRR: Die Gefahrensensoren
PRR sind eine vielfältige Klasse von Rezeptoren, die PAMP und DAMP detektieren. Unter den PRR sind die Toll-like Receptors (TLR) und die NOD-like Receptors (NLR) besonders wichtig für ihre Fähigkeit, Entzündungs- und antivirale Reaktionen einzuleiten.
- Das Inflammasom: Ein zentraler Proteinkomplex in der Entzündungsreaktion
Inflammasome sind zytosolische Proteinkomplexe, die eine zentrale Rolle bei der Regulierung von Entzündungen spielen. Ihre Aktivierung durch PAMP, DAMP oder andere Stresssignale führt zur Reifung und Sekretion proinflammatorischer Zytokine, insbesondere IL-1β und IL-18.
Interaktionsmechanismen und Signalwege
Das Verständnis der Interaktionsmechanismen zwischen PAMP, DAMP, PRR und Inflammasomen sowie der beteiligten Signalwege ist entscheidend, um die Komplexität der angeborenen Immunantwort zu entschlüsseln. Diese orchestrierten Interaktionen lösen eine Reihe von zellulären Ereignissen aus, die zur Aktivierung spezifischer und adaptiver Immunantworten führen.
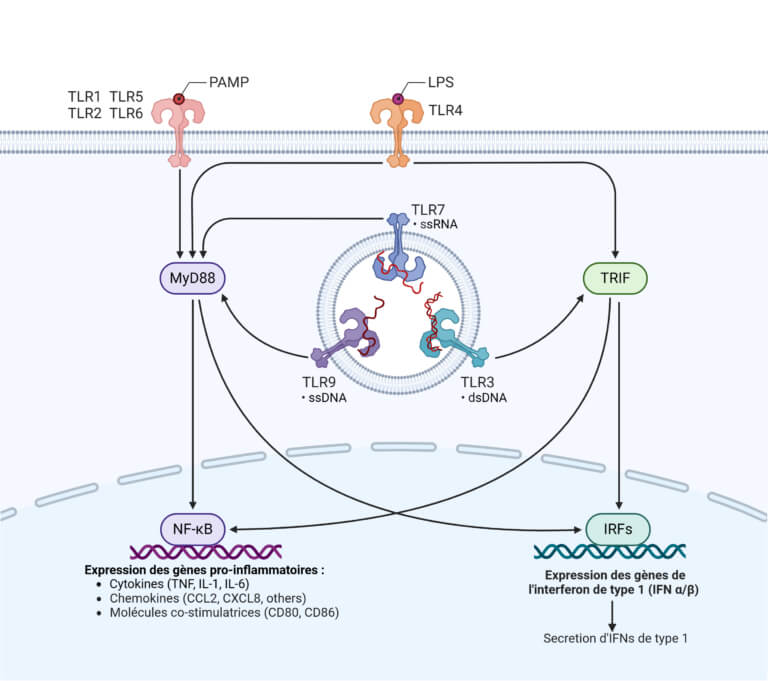
Aktivierung der PRR durch PAMP und DAMP
PRR wie TLR und NLR erkennen spezifisch PAMP und DAMP, was eine intrazelluläre Signalkaskade auslöst. TLR befinden sich beispielsweise auf der Zelloberfläche oder in Endosomen und erkennen spezifische Muster von PAMP und DAMP. Die Bindung eines TLR durch seinen Liganden führt zur Aktivierung des MyD88-abhängigen oder TRIF-abhängigen Weges, was in der Translokation des Transkriptionsfaktors NF-κB in den Kern und der Expression proinflammatorischer Gene resultiert.
Rolle der NLR und die Aktivierung des Inflammasoms
NLR spielen eine zentrale Rolle bei der Bildung des Inflammasoms. Die Aktivierung von NLRP3, einem Mitglied der NLR-Familie, durch PAMP, DAMP oder zelluläre Stresssignale führt zum Zusammenbau des NLRP3-Inflammasoms. Dieser Komplex rekrutiert den Adaptor ASC und die Pro-Caspase-1, was die Umwandlung von Pro-Caspase-1 in aktive Caspase-1 erleichtert. Caspase-1 katalysiert anschließend die Reifung von IL-1β und IL-18, zentralen Zytokinen bei der Vermittlung der Entzündungsreaktion.
Nachgeschaltete Signalübertragung und Immunantworten
Die der Aktivierung von PRR und Inflammasom nachgeschaltete Signalübertragung umfasst mehrere Wege, einschließlich des JAK-STAT-Weges, der für die Produktion von Typ-I- und Typ-II-Interferonen (IFN) als Reaktion auf virale Infektionen essenziell ist. Diese Wege tragen zu einem antiviralen Zustand bei, stimulieren die Antigenpräsentation und erleichtern die Kommunikation zwischen angeborener und adaptiver Immunität.
Regulierung der Immunantworten
Die Regulierung dieser Antworten erfolgt durch negative Feedback-Mechanismen und posttranslationale Modulatoren, die sicherstellen, dass die Immunantwort proportional zur Bedrohung ist und übermäßige Schäden am Wirtsgewebe vermieden werden. Proteine der SOCS-Familie werden beispielsweise durch Zytokine induziert und hemmen die JAK-STAT-Signalübertragung, um Entzündungsreaktionen zu begrenzen.
Klinische Implikationen und Perspektiven:
Das vertiefte Verständnis der Interaktion zwischen PAMP, DAMP, PRR und Inflammasomen eröffnet vielversprechende Wege für die Entwicklung neuer therapeutischer Strategien. Der BI(G)MED-Ansatz zur Modulation dieser Interaktionen verbessert die Immunantworten gegen Infektionen, reduziert pathologische Entzündungsreaktionen und fördert die Gewebereparatur.
Zur weiteren Vertiefung finden Sie hier einige bedeutende Publikationen auf diesem Gebiet:
- Janeway CA Jr, Medzhitov R. „Innate Immune Recognition.“ Annual Review of Immunology. 2002;20:197-216.
Ein grundlegender Artikel, der beschreibt, wie das Immunsystem Krankheitserreger durch PRRs erkennt. - Kumar H, Kawai T, Akira S. „Pathogen Recognition by the Innate Immune System.“ International Reviews of Immunology. 2011;30(1):16-34.
Dieser Artikel bietet einen umfassenden Überblick über die Erkennung von Pathogenen durch das angeborene Immunsystem mit Schwerpunkt auf den PRRs. - Takeuchi O, Akira S. „Pattern Recognition Receptors and Inflammation.“ Cell. 2010;140(6):805-820.
Ein Schlüsselartikel über die Rolle von Mustererkennungsrezeptoren bei der Initiierung von Entzündungsreaktionen. - Medzhitov R. „Origin and Physiological Roles of Inflammation.“ Nature. 2008;454:428-435 .
Untersucht die Ursprünge und physiologischen Rollen von Entzündungen und bietet einen wichtigen Kontext für das Verständnis der Aktivierung von Inflammasomen. - Schroder K, Tschopp J. „The Inflammasomes.“ Cell. 2010;140(6):821-832.
Eine grundlegende Übersicht über Inflammasome, ihren Wirkmechanismus und ihre Bedeutung bei menschlichen Krankheiten. - Latz E, Xiao TS, Stutz A. „Activation and Regulation of the Inflammasomes.“ Nature Reviews Immunology. 2013;13(6):397-411.
Beschreibt detailliert die Aktivierung und Regulierung von Inflammasomen und unterstreicht deren zentrale Rolle in der angeborenen Immunität. - Rock KL, Latz E, Ontiveros F, Kono H. „The Sterile Inflammatory Response.“ Annual Review of Immunology. 2010;28:321-342.
Dieser Artikel untersucht die sterile Entzündungsreaktion, einschließlich der Rolle von DAMPs bei der Initiierung von Entzündungen ohne das Vorhandensein von Pathogenen. - Bianchi ME. „DAMPs, PAMPs and Alarmins: All We Need to Know About Danger.“ Journal of Leukocyte Biology. 2007;81(1):1-5.
Ein aufschlussreicher Überblick über Gefahrenmoleküle, einschließlich DAMPs und PAMPs, und ihre Bedeutung für die Immunantwort.